【中3理科】イオンについてわかりやすく!
そもそもイオンって何??
簡単に言うと、イオンとは電気を帯びているものだと考えましょう!
よく原子とイオンの違いがわからない人がいますが…
原子は電気を帯びていない
イオンは電気を帯びている
この違いだけ抑えておけば大丈夫です!
なぜ原子は電気を帯びていないの?
原子核の中にあるプラスの電気を帯びた陽子と原子核の外をクルクル回るマイナスの電気を帯びた電子の個数が等しいからです!
そのため原子の状態では必ず電気的に中性であり電気は帯びていません。
また中性子も陽子と同様に原子核の中に存在します。
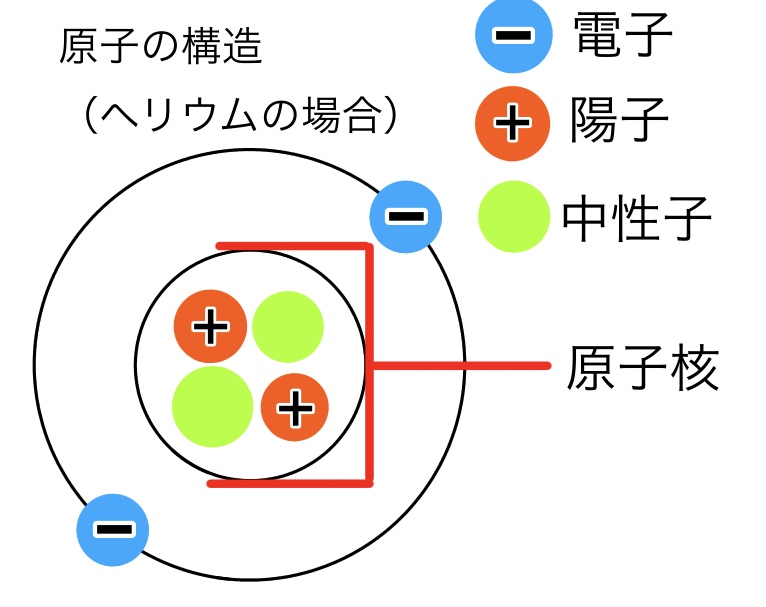
ヘリウム原子の場合、陽子が2個と電子が2個あるので電気は帯びていません。
なぜイオンは電気を帯びているの?
結論から言うと
イオンとは原子に含まれる電子が移動することによってイオンとなります!
因みに移動の仕方は2パターン!
電子がくっつくか、離れるか!
これだけ!
それって電気を帯びる答えなのか?
と思われそうなので…こちらの図をご覧ください!

例えば、水素原子(H)ではマイナスの電気を帯びた電子を1つ失うので、プラスの電気を帯びた陽子が1つ多く存在することになりますよね!(原子は必ず電子と陽子の数が等しいから!)
そのため電気的にプラスになり、水素イオン(H+)となります!
つまり、電子がはなれれば陽イオン、電子がくっつけば陰イオンということになります!
イオンの中でも…
プラスの電気を帯びるものを陽イオン
マイナスの電気を帯びているものを陰イオンと言います!
 |
高校受験3カ月で理科の偏差値を30から60にする改訂新版 落ちこぼれからの大逆転!! (Yell books) [ 小野博司 ] 価格:1,620円 |
![]()
電解質と非電解質
電解質
・水に溶けた時に電気が流れる物質
非電解質
・水に溶けた時に電気が流れない物質
この区別くらいは皆さんはすぐにわかるかと思います!
実際に覚えなければいけないのは電解質と非電解質が具体的にどんな物質があるのか、ということです!
うわー、めんどくさそーと思うかもしれませんが…
皆さんが覚えるのは非電解質のみ!!
さらに、覚えるべき非電解質はこの3つ!
これ以外は電解質と考えてもらって結構です!
もちろん、これ以外にも存在しますが、中学理科ではこの3つを覚えていれば十分です!
例えば、砂糖の溶けた水は電気を通さないのに対し、食塩水は電気を通すということです!
電離
電離とは電解質が水に溶けた時に陽イオンと陰イオンに分かれることを言います
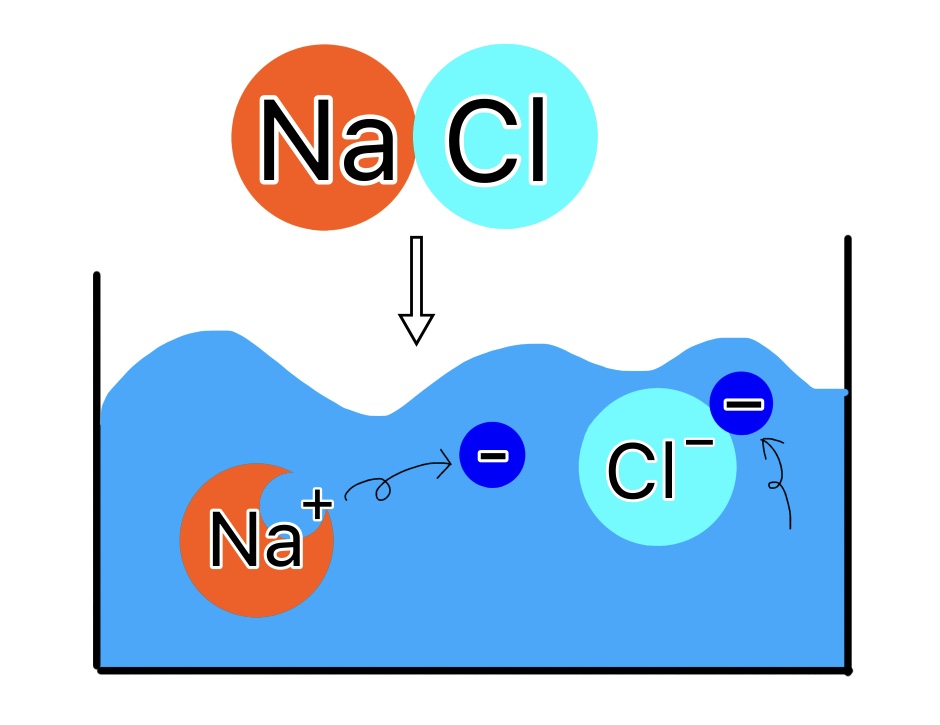
つまり陽イオンと陰イオンに分かれなければ電気が流れることはないということです。
先程、非電解質は3つだけで十分と述べましたがこのような問題には注意
答えは1,2,5
塩素を選んではいけない理由

このように塩素は水に溶けても陰イオンになるだけであり、電離はしないのです!
同様に水素やナトリウムなども陽イオンにしかならないため水に溶かしても電気が流れることはありません!
ここも合わせて覚えておいてください!
 |
価格:1,296円 |
![]()
補足
水は電気を通すと思われがちですが、一般的に水は電気を通しません。しかし水道水は電気を通します。
なぜならば、電解質を含んでいるから!
但し、理科的な用語で蒸留水という言葉が出てきたら、これは電気を通しません!
 |
価格:1,309円 |
![]()
まず把握して欲しいのがこちら
これらは必ず暗記してください!
まずはこちらの絵をご覧ください!

このように、イオン式では元素記号の右上にプラスかマイナスの記号が付きます。
もちろん
プラスであれば陽イオン
マイナスであれば陰イオンを示します!
プラスやマイナスの横に付いている数字については電子の移動した個数を示しています!!
例えば、陽イオンの場合は上記で示した通り電子を失うことで陽イオンとなります。
2+と記してあれば、電子を2つ失ってできた陽イオンということになります!
陰イオンでも同じ事が言えます!
どうでしたか?
イオンについて少しは理解していただけたでしょうか?
イオンについては中学理科の中でもかなり重たい内容であると思いますので、これからも記事を書き足して行く予定です!